باتریهای قابل شارژ Li-S (لیتیوم-گوگرد) به دو دلیل پتانسیل تجاری بالایی دارند؛ ابتدا اینکه گوگرد به مقدار کافی و عملا بهصورت آزاد در دسترس بوده و یک ماده با هزینه پایین است. دوم، انرژی گیبس واکنش لیتیوم (Li) و گوگرد تقریبا Wh/kg 2600 است (با فرض واکنش کامل لیتیوم با گوگرد و تشکیل Li2S). با این دو مزیت، باتریهای Li-S میتوانند هزینه پایین و چگالی انرژی بالایی (بسیار بالاتر از لیتیوم-یون) داشته باشند و پاسخگوی نیاز برای ذخیره ثابت و قابل حمل انرژی (برای وسایل نقلیه و شبکههای محاسباتی) باشند. علیرغم این مزایا، استفاده از باتریهای قابل شارژ Li-S هنوز بسیار محدود است. موانعی همچون رسانایی پایین گوگرد و از بین رفتن مواد کاتدی گوگرد بعنوان نتیجه انحلال پلیسولفید (شاتل پلیسولفیدی) وجود دارند که باعث اثر شاتل و از بین رفتن ظرفیت قابل توجهی از باتری میشوند. راهحل این معضل استفاده از مادهای است که تمام مواد فعال باتری را در کنار هم حفظ کند. پژوهشگران بهتازگی به شکل غیرمنتظرهای متوجه شدهاند که یکی از مشتقات جلبک دریایی بنام کاراگینان، میتواند به عنوان یک تثبیتکننده در این باتریها عمل کند؛ در نتیجه، ثبات بهتر، چرخههای بیشتر و طول عمر طولانیتر را به ارمغان میآورد. بنابراین ترکیب شیمیایی لیتیوم و گوگرد به صورت بالقوه میتواند یک هدف مناسب برای باتریها باشد.
طراحان باتری به شکل رایج از پلیمرهای چسبمانند که با پلیسولفید واکنش میدهد برای تثبیت پلیسولفیدها استفاده میکنند، اما محققان در این پژوهش از کاراگینان – مادهای استخراج شده از جلبکهای دریایی قرمز با گروه عاملی مشابه- استفاده کردند. این ماده با بازده بسیار مناسبی پلیسولفید را تثبیت نموده و یک الکترود بسیار پایدار ایجاد کرد. سپس پژوهشگران از پرتوهای منحصر به فرد اشعه ایکس برای نظارت بر روند واکنش تحت شرایط درجا استفاده کردند.
یافتههای تحقیقات این دانشمندان به وسیله جنرال موتورز به عنوان یک شریک تجاری نیز مورد تایید قرار گرفته است. آنها قصد دارند با بهبود این سیستم به هزاران سیکل برسند. این باتریها بسیار سبک هستند و بنابراین به شکل بالقوه برای هواپیماها و پهبادها کاربرد دارند.
شاتل پلیسولفیدی دلیل اصلی عدم موفقیت در تولید چرخههای بیشتری در باتری لیتیوم-گوگرد (Li-S) بوده است. در اینجا یک واکنش جایگزینی نوکلئوفیلی بین گروههای عملکردی نگهدارندهها و پلیسولفیدها میتواند به شکل غیرمنتظرهای باعث پایداری پلیسولفیدها شود. این واکنش جایگزینی توسط طیف قابل مشاهده فرابنفش (UV) و طیف فوتوالکترونی اشعه ایکس تایید شده است. نظارت بر پایداری پلیسولفید توسط طیفهای جذبی اشعه ایکس سینکروترون k-edge مربوط به گوگرد، در محل (in situ) صورت گرفته است. الکترودهای حاصل ظرفیت اولیهای تا مقدار mAh/cm2 20.4 نشان میدهند. گوگرد در ابعاد میکرون در حین ایجاد چرخه باتری به پوشش لایهای در مقیاس نانو روی نگهدارنده کاتدی تبدیل میشود. استفاده مستقیم از گوگرد در ابعاد نانو امکان ایجاد ظرفیت بیشتر تا mAh/cm2 33.7 را میدهد. که این مقدار بیشترین ظرفیت برحسب مساحت است که در باتری Li-S گزارش شده است. این افزایش عملکرد بهخاطر کاهش اثر شاتل از طریق ایجاد پیوند اشتراکی بین پلیسولفید با نگهدارنده پلیمری است.
بهصورت تئوری، اوکتاسولفور (سیکلو-S8) حین لیتیاسیون در کاتد گوگرد، بهصورت گامبهگام به Li2S جامد کاهش مییابد. در حین این فرآیند، هرگاه مقدار x از 8 تا 4 تغییر کند، الکترولیت Li2Sx قابلحل تولید میشود. لیتیوم پلیسولفید قابل حل، درون الکترولیت منتشر شده و در ادامه در سمت فلز لیتیوم برای تشکیل مرتبه پایین پلیسولفید، کاهش مییابد. پلیسولفیدهایی که نسبتا کاهش یافتهاند و قابلحل هستند میتوانند در جهت عکس به سمت الکترود گوگرد منتشر شوند. پلیسولفیدها در حین فرآیند دیلیتاسیون در سمت کاتد به مرتبه بالاتری از پلیسولفیدها اکسید شدهاند. این اثر شاتل (منظور حرکت پلیسولفیدها بین دو الکترود لیتیوم و گوگرد است.)، به همراه رسانایی ضعیف، منجر به امکان بهرهگیری پایین از گوگرد و از دست رفتن سریع ظرفیت میشود. این موارد مانع از استفاده گستردهی باتریهای قابل شارژ Li-S شده است.
پلیمرهایی مانند ژلاتین، اکسید پلیاتیلن، پلیاکریلیک اسید، نگهدارنده چسب صمغ عربی بعنوان نگهدارندههای مطمئن برای حل این مسئله شناخته شدند. علاوه بر خواص بهتر توزیع و انتشار نگهدارندههای نوظهور، وجود گروههای کربونیل در این نگهدارندهها نقش اساسی در بهبود اجرای چرخه باتری ایفا میکند. اکسیژن دارای الکترون فراوان با جفتهای تنها، شرایط مساعدی را برای تشکیل پیوند لیتیوم-اکسیژن (Li-O) با لیتیوم پلیسولفید فراهم میآورد. مشارکت گروههای کربونیل و اثر اصلاح سطح برای گروه تحقیقاتی این پژوهش نیز اثبات شد.
یک روش جایگزین برای ایجاد نگهدارنده قوی برای پلیسولفید، ایجاد پیوند اشتراکی بین الکترود و نمونههای گوگرد است. واکنش جانشینی هستهدوستی (نوکلئوفیلی) بین پلیسولفیدهای حلشده و گروههای ترککننده روی نگهدارنده پلیمری میتواند پلیسولفیدها را بوسیله پیوند اشتراکی جدید C-S روی الکترود ثابت نگه دارد. چند عامل تعیینکننده واکنشپذیری در واکنش هستهدوستی هستند: توانایی نوکلئوفیل و گروه ترککننده برای قطبیشدن، پایداری گروه ترککننده، برهمکنش بین نوکلئوفیل و گروه ترککننده. انتخاب گروه ترککننده برای حفظ بهموقع پلیسولفید بسیار مهم است. یک گروه ترککننده خوب باید بتواند یک بار بزرگ منفی را در هر دو حالت وضعیت گذار و مرحله تولید تثبیت کند. معیار خوب برای پایداری آنیون، pka یک اسید کانژوگه مرتبط با یک آنیون است. بدین معنی که pka پایینتر، مربوط به یک گروه ترککننده بهتر بوده است. همچنین با توجه به شرایط منحصر به فرد باتریهای Li-S، گروه ترککننده نباید گونههای واکنشی را به سیستم وارد کند. براساس این الزامات، گروه ترککننده سولفاتی قابل پذیرش است (تصویر1). پلیوینیلسولفات مصنوعی (PVS)، یک پلیمر مصنوعی رایج، یک ساختار غنی شیمیایی سولفاتی دارد که میتواند به خوبی کنترل شود و یک پلیمر ایدهآل برای تشکیل یک کامپوزیت است. اگرچه، استحکام پیوند PVS زمانیکه بعنوان نگهدارنده برای تشکیل یک الکترود کامپوزیت استفاده شود، به مقدار لازم کافی نیست. درمقابل، کاراگینان ، مادهای که از پلیساکاریدها در جلبک دریایی مشتق میشود، ویژگیهای دلخواه برای یک نگهدارنده را دارد؛ از قبیل: حلالیت در آب، چسبندگی بالا، غلظت متغیر گروه ترککننده سولفاتی، زیستتخریب پذیری و غیر سمی بودن.
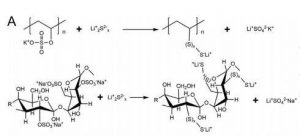
تصویر1- پلیمرها با گروههای ترککننده شیمیایی میتوانند با پلیسولفید واکنش دهند. در این تصویر ساختار مولکولی PVS و محصول طبیعی کاراگینان و واکنشهای جابهجایی آنها با پلیسولفید را برای تشکیل پلیسولفیدهای تثبیتشده روی پلیمرها مشاهده میکنید.
چگالی گروههای سولفاتی در کاراگینان فرایند سفتشدن را کنترل میکند و گروههای هیدروکسیل گسترش یافته فاقد ساختار پلیساکارید بوده و ارتباط گستردهای با محیطهای آبی قطبی برقرار میکنند. طبیعت بهطور اتفاقی کاراگینان طراحیشده را بعنوان یک ماده ایدهآل جهت استفاده بعنوان نگهدارنده الکترودهای گوگردی دارد. این ماده نهتنها گروههای ترککننده سولفاتی را برای تثبیت سولفیدها دارد، بلکه گروههای غنی هیدروکسیل را نیز بهجهت چسبندگی برای تشکیل شبکههای رسانای پایدار با افزودنیهای رسانای کربن سیاه و برهمکنش با الکترولیت قطبی دارا میباشد. کاراگینان چسبندگی و عملکرد سولفاتی بسیار بالاتری بعنوان یک گروه ترککننده دارد. بهدلیل بعضی از گروههای سولفاتی روی نواحی کربن اولیه، کاراگینان حتی باید واکنشپذیری شیمیایی بهتری نسبت به PVS با پلیسولفیدها داشته باشد.
در مورد جزئیات واکنش جانشینی نوکلئوفیلی و نحوه تاثیرگذاری آن بر عملکرد باتری در شمارههای بعدی بیشتر توضیح خواهیم داد.


